Antraz
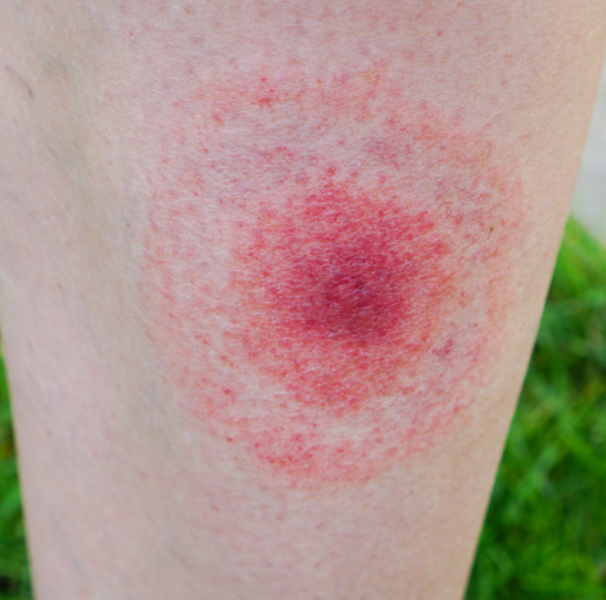
Antraz (Carbúnculo) O antraz é uma zoonose infecciosa aguda causada pela bactéria Bacillus anthracis. Embora raro, é uma doença grave e potencialmente fatal, especialmente nas formas inalatória e gastrointestinal. Pode ocorrer de forma cutânea, pulmonar, digestiva ou meníngea, dependendo da via de exposição aos esporos da bactéria. O antraz ganhou notoriedade como agente de bioterrorismo devido à sua elevada letalidade quando inalado e à capacidade de formar esporos extremamente resistentes no ambiente. Agente Etiológico Bacillus anthracis O Bacillus anthracis é um coco-bacilo Gram-positivo, aeróbico, formador de esporos e encapsulado. A cápsula de polipeptídeo e a toxina antráxica (composta por três proteínas: fator letal, fator do edema e antígeno protetor) são os principais determinantes de virulência. Os esporos são altamente resistentes e podem sobreviver por décadas no solo contaminado. Epidemiologia O antraz é mais comum em regiões com práticas agropecuárias precárias, onde o solo é contaminado com esporos da bactéria. Afeta principalmente herbívoros (bovinos, ovinos, caprinos) e ocasionalmente humanos que manipulam animais ou produtos contaminados. Distribuição mundial: África Subsaariana, Ásia Central, América do Sul e partes do Oriente Médio No Brasil: Casos humanos são raros, mas ocorrem surtos esporádicos em áreas rurais, especialmente no Norte e Nordeste Transmissão humana: contato com esporos por via cutânea (mais comum), inalatória, digestiva ou inoculação acidental em laboratórios Mortalidade: Cutânea tratada: <1% Inalatória ou meníngea: até 85% se não tratada Perfil típico: Trabalhadores rurais, curtidores de couro, manipuladores de lã ou peles de animais, veterinários, trabalhadores de laboratório Principais Reservatórios Animais herbívoros infectados (bovinos, ovinos, caprinos, cavalos) Solo contaminado com esporos (especialmente em locais de morte de animais não incinerados) Produtos de origem animal contaminados (lã, couro, carne mal cozida) Transmissão para humanos: Cutânea: contato direto com pele ferida ou mucosas e esporos Inalatória: inalação de esporos em ambientes contaminados (ex: lã, feno) Gastrointestinal: ingestão de carne mal cozida de animal infectado Inoculação acidental: em laboratórios ou bioterrorismo Ciclo de Vida No ambiente, o Bacillus anthracis existe como esporo. Quando ingerido ou inalado por animais, os esporos germinam no organismo e se transformam em formas vegetativas que se multiplicam rapidamente e produzem toxinas. Após a morte do hospedeiro, se exposto ao oxigênio, o bacilo esporula novamente, reiniciando o ciclo. Quadro Clínico O antraz pode se apresentar em quatro formas clínicas principais: cutânea, inalatória, gastrointestinal e meníngea. Cada uma tem apresentação e gravidade distintas, sendo a forma cutânea a mais comum e a inalatória/meníngea, as mais letais. Forma Cutânea Surge após contato da pele lesionada com esporos. A bactéria invade a derme, formando uma pápula indolor que evolui para vesícula e depois uma úlcera com crosta escura (“carbúnculo”). Sinais e sintomas: Pápula pruriginosa → vesícula → úlcera central necrótica (“eschar”) Edema local e linfadenopatia regional Lesão indolor, mas com edema acentuado Febre baixa, mal-estar (em casos mais extensos) Forma Inalatória (Pulmonar) Inalação de esporos, que germinam nos linfonodos mediastinais. Evolui com mediastinite hemorrágica e insuficiência respiratória. Sinais e sintomas: Febre, mal-estar, tosse seca Dispneia progressiva, dor torácica Sudorese intensa Edema mediastinal (em imagem) Hipoxemia e choque Hemorragia pulmonar e morte em 1–2 dias se não tratado Forma Gastrointestinal Resulta da ingestão de carne mal cozida de animal infectado. Leva à ulceração do trato digestivo com sepse. Sinais e sintomas: Náuseas, vômitos, dor abdominal intensa Diarreia com ou sem sangue Febre alta Ascite hemorrágica (em casos graves) Sepse e falência de múltiplos órgãos Forma Meníngea (secundária ou isolada) Ocorre como complicação da forma inalatória, cutânea ou gastrointestinal. A evolução é fulminante. Sinais e sintomas: Cefaleia intensa Vômitos, rigidez de nuca Rebaixamento do nível de consciência Convulsões Hemorragia subaracnoidea Mortalidade altíssima (>90%) Surge após contato da pele lesionada com esporos. A bactéria invade a derme, formando uma pápula indolor que evolui para vesícula e depois uma úlcera com crosta escura (“carbúnculo”). Sinais e sintomas: Pápula pruriginosa → vesícula → úlcera central necrótica (“eschar”) Edema local e linfadenopatia regional Lesão indolor, mas com edema acentuado Febre baixa, mal-estar (em casos mais extensos) Inalação de esporos, que germinam nos linfonodos mediastinais. Evolui com mediastinite hemorrágica e insuficiência respiratória. Sinais e sintomas: Febre, mal-estar, tosse seca Dispneia progressiva, dor torácica Sudorese intensa Edema mediastinal (em imagem) Hipoxemia e choque Hemorragia pulmonar e morte em 1–2 dias se não tratado Resulta da ingestão de carne mal cozida de animal infectado. Leva à ulceração do trato digestivo com sepse. Sinais e sintomas: Náuseas, vômitos, dor abdominal intensa Diarreia com ou sem sangue Febre alta Ascite hemorrágica (em casos graves) Sepse e falência de múltiplos órgãos Ocorre como complicação da forma inalatória, cutânea ou gastrointestinal. A evolução é fulminante. Sinais e sintomas: Cefaleia intensa Vômitos, rigidez de nuca Rebaixamento do nível de consciência Convulsões Hemorragia subaracnoidea Mortalidade altíssima (>90%) A infecção começa com a germinação dos esporos no tecido hospedeiro, formando bacilos vegetativos que liberam toxinas letais. As toxinas provocam necrose tecidual, edema e choque. A cápsula evita fagocitose. A forma cutânea se restringe à pele; a inalatória leva à mediastinite hemorrágica; a gastrointestinal provoca úlceras intestinais e a meníngea causa inflamação severa das meninges com hemorragia. Diagnóstico A confirmação laboratorial depende da identificação direta da bactéria ou de testes moleculares. A suspeita clínica, especialmente em contextos de risco ocupacional, é fundamental. Métodos diagnósticos: Cultura de secreções, sangue ou LCR Meio de ágar sangue Rápida positividade em 24–48h Coloração de Gram: bacilos Gram-positivos grandes em cadeia PCR: sensível e rápida (usada em suspeitas de bioterrorismo) Sorologia: útil em investigações retrospectivas Hemograma: leucocitose importante Imagem (forma inalatória): alargamento mediastinal e derrame pleural Conduta diante de suspeita: Notificação imediata Início de antibióticos sem aguardar confirmação Isolamento respiratório e medidas de biossegurança Acompanhamento A maioria dos casos cutâneos não complicados pode ser acompanhada ambulatorialmente, com antibióticos orais. Formas sistêmicas exigem internação imediata, muitas vezes em UTI, com suporte hemodinâmico e respiratório. Monitoramento rigoroso da função renal, hepática, coagulograma e vigilância para sepse são fundamentais. Tratamento O tratamento precoce com antibióticos é crucial. Formas graves exigem associação de antimicrobianos parenterais e, quando possível, uso de antitoxinas específicas. Se Meningite Antibioticoterapia: Ciprofloxacino 400 mg EV de 8/8 horas; Associar