Antraz
Infecção bacteriana zoonótica causada pelo Bacillus anthracis, transmitida principalmente pelo contato com animais infectados, carcaças, couro, lã ou produtos de origem animal contaminados por esporos.
♙ O que é
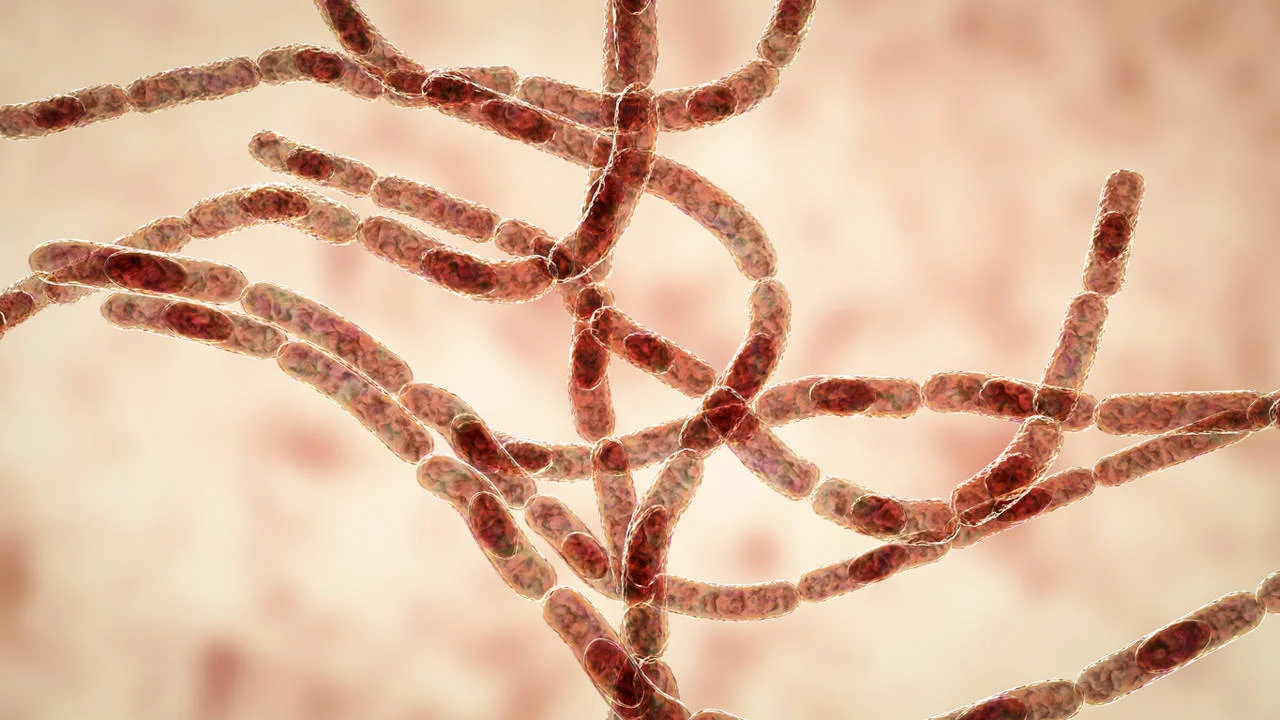
O antraz, também chamado de carbúnculo, é uma zoonose infecciosa aguda causada pela bactéria Bacillus anthracis. Embora seja uma doença rara em humanos, pode ser grave e potencialmente fatal, principalmente nas formas inalatória, gastrointestinal e meníngea.
A doença ocorre após exposição aos esporos da bactéria, podendo se manifestar na forma cutânea, pulmonar, digestiva ou meníngea. O antraz também ganhou importância histórica por seu potencial uso como agente de bioterrorismo.
♧ Agente etiológico
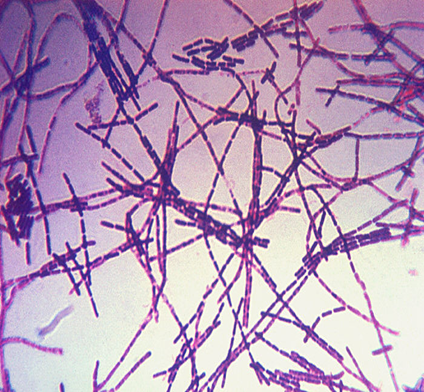
O agente causador do antraz é o Bacillus anthracis, um coco-bacilo Gram-positivo, aeróbico, encapsulado e formador de esporos.
- Esporos resistentes: podem sobreviver por décadas no solo contaminado.
- Cápsula polipeptídica: ajuda a bactéria a escapar da fagocitose.
- Toxina antráxica: composta por fator letal, fator do edema e antígeno protetor.
- Alta virulência: especialmente nas formas sistêmicas e inalatórias.
◎ Epidemiologia
O antraz é mais comum em regiões com práticas agropecuárias precárias, onde há contaminação ambiental por esporos. Afeta principalmente herbívoros, como bovinos, ovinos, caprinos e cavalos, podendo atingir humanos expostos a animais ou produtos contaminados.
África Subsaariana, Ásia Central, América do Sul e Oriente Médio.
Casos humanos raros, com surtos esporádicos em áreas rurais.
Baixa na forma cutânea tratada; alta nas formas inalatória e meníngea.
Trabalhadores rurais, veterinários, curtidores e manipuladores de lã/couro.
A forma cutânea é a apresentação mais frequente.
⚕ Reservatórios e transmissão
Principais reservatórios
- Animais herbívoros infectados, como bovinos, ovinos, caprinos e cavalos.
- Solo contaminado por esporos, especialmente após morte de animais infectados.
- Produtos de origem animal contaminados, como lã, couro, peles e carne.
Formas de transmissão para humanos
- Contato cutâneo com pele lesionada ou mucosas expostas a esporos.
- Inalação de esporos presentes em ambientes ou produtos animais contaminados.
- Ingestão de carne mal cozida de animal infectado.
- Inoculação acidental em laboratório ou exposição intencional.
♧ Ciclo de vida e fisiopatologia
No ambiente, o Bacillus anthracis permanece na forma de esporo. Após entrada no organismo, os esporos germinam e se transformam em formas vegetativas, que se multiplicam rapidamente e liberam toxinas.
Essas toxinas provocam edema, necrose tecidual, inflamação intensa e choque. Após a morte do hospedeiro, se houver exposição ao oxigênio, a bactéria pode esporular novamente e contaminar o ambiente.
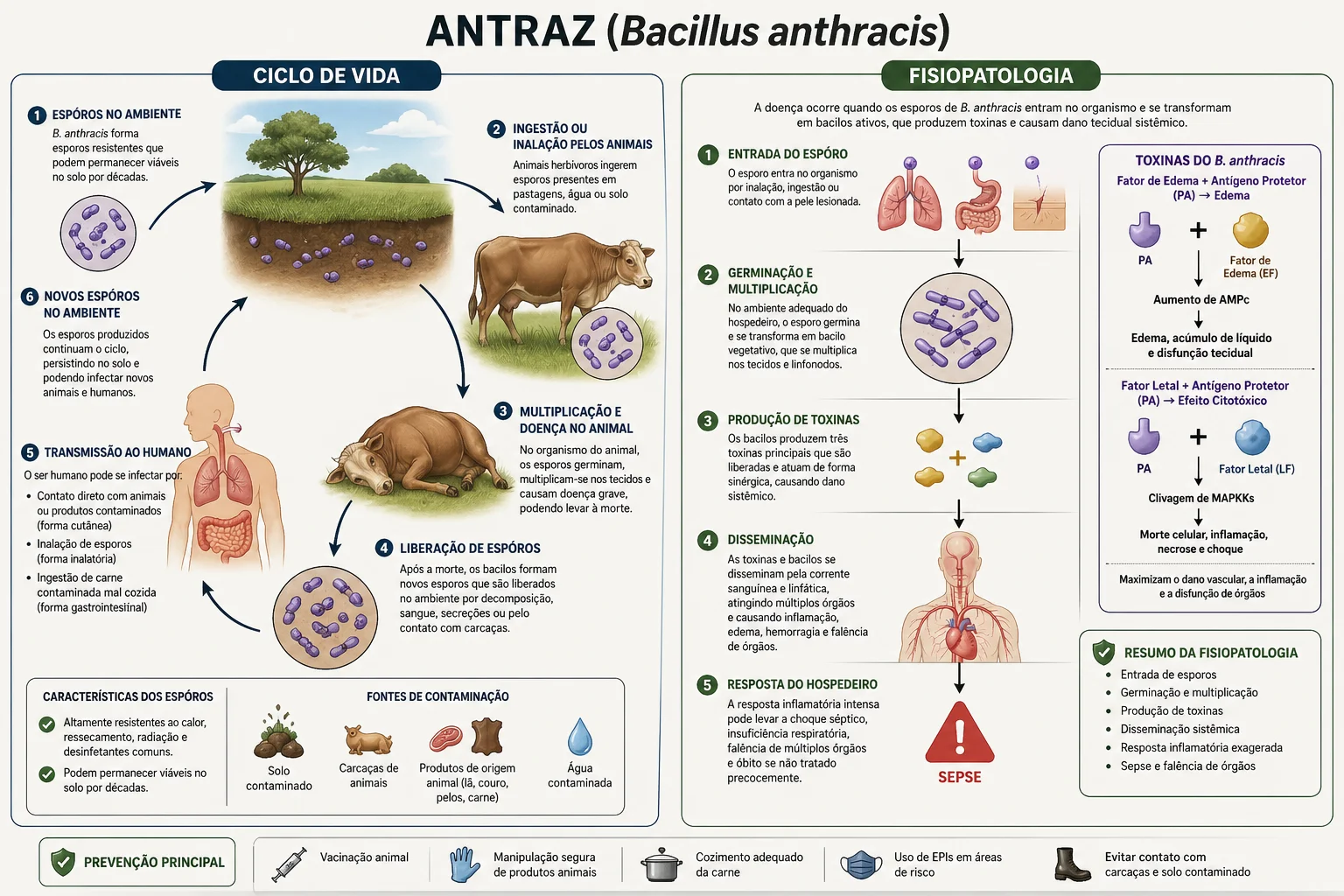 Clique na imagem para ampliar
Clique na imagem para ampliar
⚕ Como ocorre a transmissão
A transmissão do antraz ocorre pela exposição aos esporos do Bacillus anthracis. Esses esporos podem penetrar no organismo pela pele lesionada, pelas vias respiratórias, pelo trato gastrointestinal ou por inoculação acidental.
▣ Principais vias de infecção
Ocorre pelo contato de pele ferida ou mucosas com esporos presentes em animais, carcaças, couro, lã ou solo contaminado.
Resulta da inalação de esporos em ambientes contaminados, sendo uma das formas mais graves da doença.
Está associada à ingestão de carne mal cozida proveniente de animal infectado.
Pode ocorrer em laboratórios ou em situações de exposição intencional, como bioterrorismo.
♙ Grupos de maior risco
- Trabalhadores rurais.
- Veterinários e profissionais que lidam com animais.
- Manipuladores de lã, couro, peles ou carcaças.
- Trabalhadores de abatedouros e curtumes.
- Profissionais de laboratório.
- Pessoas expostas a carne de procedência duvidosa em áreas endêmicas.
♧ Quadro clínico
O antraz pode se apresentar em quatro formas clínicas principais: cutânea, inalatória, gastrointestinal e meníngea. A gravidade depende da via de exposição, da carga de esporos e da rapidez do diagnóstico e tratamento.
◎ Formas clínicas
Inicia como pápula ou vesícula, evoluindo para úlcera com escara negra, geralmente indolor e com edema ao redor.
Começa com sintomas inespecíficos, como febre, mal-estar e tosse, podendo evoluir rapidamente para dispneia e choque.
Pode causar dor abdominal, náuseas, vômitos, diarreia, febre e evolução sistêmica grave.
Forma grave, geralmente secundária à disseminação hematogênica, com meningite hemorrágica e alta letalidade.
▣ Sinais de gravidade
- Febre alta e toxemia.
- Dispneia, dor torácica ou insuficiência respiratória.
- Alteração do nível de consciência.
- Sinais meníngeos.
- Hipotensão, choque ou sepse.
- Edema extenso ou lesão cutânea rapidamente progressiva.
▣ Suspeita diagnóstica
O diagnóstico deve ser suspeitado diante de quadro clínico compatível associado à exposição ocupacional, contato com animais ou produtos de origem animal contaminados, ingestão de carne suspeita ou exposição laboratorial.
◎ Exames utilizados
Pode ser realizada em secreções de lesões, sangue ou líquor, com crescimento em ágar sangue.
Mostra bacilos Gram-positivos grandes, frequentemente em cadeia.
Exame rápido e sensível, útil especialmente em casos graves ou suspeita de exposição intencional.
Na forma inalatória, pode haver alargamento mediastinal e derrame pleural.
⚕ Conduta diante de suspeita
- Notificação imediata às autoridades de saúde.
- Início de antibioticoterapia sem aguardar confirmação laboratorial em casos suspeitos.
- Coleta de amostras antes do antibiótico, quando possível, sem atrasar tratamento.
- Medidas de biossegurança conforme forma clínica e contexto epidemiológico.
- Avaliação hospitalar imediata nas formas sistêmicas, inalatória, gastrointestinal ou meníngea.
✦ Princípios do tratamento
O tratamento do antraz deve ser iniciado precocemente, sem aguardar confirmação laboratorial quando houver suspeita clínica e epidemiológica. Formas sistêmicas, inalatórias, gastrointestinais ou com suspeita de meningite exigem internação, antibioticoterapia venosa combinada, suporte intensivo e, quando disponível, terapia adjuvante com antitoxina.
🧠 Se meningite
Na suspeita ou confirmação de meningite por antraz, deve-se utilizar esquema venoso combinado com boa penetração em sistema nervoso central.
Ciprofloxacino: 400 mg EV de 8/8 horas.
Associar com Meropeném: 2 g EV de 8/8 horas.
Associar com Linezolida: 600 mg EV de 12/12 horas.
Manter tratamento venoso por 2 a 3 semanas ou até estabilidade clínica. Após estabilização, completar o esquema até 2 meses de tratamento com:
500 mg VO de 12/12 horas.
100 mg VO de 12/12 horas.
💉 Tratamento adjuvante
Nas formas sistêmicas graves, especialmente meningite, forma inalatória ou doença disseminada, deve-se associar terapia adjuvante antitoxina, quando disponível.
40 mg/kg EV, diluído em SF 0,9% ou 0,45%, em dose única. Infundir em 2 horas. Administrar anti-histamínico antes da infusão.
Anthrasil — 60 unidades/frasco: 7 frascos EV, infundidos em 0,5 mL/minuto, máximo de 2 mL/minuto.
🏥 Descartada meningite
Quando a meningite é descartada, o tratamento das formas sistêmicas pode ser feito com ciprofloxacino associado a um inibidor de síntese proteica.
Ciprofloxacino: 400 mg EV de 8/8 horas.
Associar com Clindamicina: 900 mg EV de 8/8 horas.
OU Linezolida: 600 mg EV de 12/12 horas.
Manter tratamento venoso por 2 a 3 semanas ou até estabilidade clínica. Após estabilização, completar até 2 meses de tratamento com:
500 mg VO de 12/12 horas.
100 mg VO de 12/12 horas.
↻ Alternativas terapêuticas
Alternativas ao Ciprofloxacino EV
750 mg EV de 24/24 horas.
400 mg EV de 24/24 horas.
Alternativas ao Meropeném
1 g EV de 6/6 horas.
Para cepas sensíveis: 4 milhões de unidades EV de 4/4 horas.
3 g EV de 6/6 horas.
Alternativas à Linezolida para meningite
900 mg EV de 8/8 horas.
600 mg EV de 12/12 horas.
1 g EV de 6/6 ou de 8/8 horas.
Alternativas à Linezolida ou Clindamicina quando meningite estiver excluída
200 mg EV em dose única, seguido de 100 mg EV de 12/12 horas.
600 mg EV de 12/12 horas.
💊 Alternativas orais para completar 60 dias
Após estabilidade clínica e término da fase venosa, podem ser utilizadas alternativas orais para completar o esquema total de 60 dias, conforme sensibilidade, tolerância e avaliação clínica.
750 mg VO de 24/24 horas.
400 mg VO de 24/24 horas.
600 mg VO de 8/8 horas.
Para cepas sensíveis à penicilina: 1 g VO de 8/8 horas.
Penicilina V: 500 mg VO de 6/6 horas.
👁 Seguimento
Pacientes tratados devem ser acompanhados por pelo menos 2 meses, com vigilância clínica para recidiva, complicações neurológicas, respiratórias, infecciosas e sinais de sepse. Casos pulmonares, meníngeos ou sistêmicos devem manter seguimento especializado.
◇ Complicações da brucelose
A brucelose pode comprometer diversos sistemas. As complicações são mais frequentes quando há atraso diagnóstico, tratamento inadequado ou doença prolongada.
◎ Principais acometimentos
Sacroileíte, espondilodiscite, artrite periférica e dor lombar persistente.
Endocardite é rara, mas representa a principal causa de morte relacionada à brucelose.
Neurobrucelose pode cursar com meningite, encefalite, radiculopatia ou neuropatias.
Orquite, epididimite e prostatite podem ocorrer, especialmente em homens.
Hepatomegalia, esplenomegalia, elevação de transaminases e granulomas hepáticos.
Anemia, leucopenia, plaquetopenia e alterações inflamatórias podem estar presentes.
🛡 Como prevenir
A prevenção do antraz depende do controle sanitário animal, manejo adequado de carcaças, inspeção de produtos de origem animal e uso de equipamentos de proteção por pessoas expostas.
▣ Medidas individuais
- Evitar contato direto com animais doentes ou mortos sem proteção.
- Usar luvas, máscara, botas e proteção ocular ao manipular carcaças, couro, lã ou peles.
- Consumir apenas carne inspecionada e bem cozida.
- Evitar manipular produtos animais de origem desconhecida.
- Procurar atendimento diante de lesões suspeitas após exposição ocupacional.
⚕ Medidas coletivas
Importante em regiões endêmicas para reduzir surtos em rebanhos.
Animais suspeitos não devem ser abertos; o manejo deve seguir normas sanitárias.
Fiscalização de carne, couro, lã e outros produtos de origem animal.
Casos suspeitos devem ser comunicados rapidamente aos serviços de vigilância.
Resultado final
Revisão das questões
Quadro clínico principal
- Forma cutânea: pápula → vesícula → úlcera com escara negra
- Edema importante ao redor da lesão
- Forma inalatória: febre, dispneia e dor torácica
- Forma gastrointestinal: dor abdominal, vômitos e diarreia
- Febre e mal-estar geral
- Evolução rápida em formas sistêmicas
Diagnóstico
Identificação do Bacillus anthracis em amostras clínicas
- Cultura de sangue, lesão ou secreções
- PCR para detecção rápida
- Microscopia (bacilos gram-positivos)
- Imagem em casos pulmonares (alargamento mediastinal)
- História epidemiológica é fundamental
Tratamento
Antibioticoterapia precoce é essencial
- Ciprofloxacino ou doxiciclina como base
- Associação com outros antibióticos em casos graves
- Tratamento prolongado (até 60 dias em exposição inalatória)
- Suporte intensivo em formas sistêmicas
Complicações
- Sepse e choque séptico
- Mediastinite hemorrágica
- Meningite por antraz
- Insuficiência respiratória grave
- Alta mortalidade nas formas inalatória e sistêmica
Importante
O antraz pode evoluir rapidamente para formas sistêmicas graves, especialmente quando há inalação de esporos, podendo causar sepse, meningite, insuficiência respiratória e alta mortalidade se não tratado precocemente.
Referências bibliográficas
Ver todas as referências utilizadas neste artigo
Referências bibliográficas
- Centers for Disease Control and Prevention (CDC). Anthrax. Clinical information and guidance.
- World Health Organization (WHO). Anthrax in humans and animals. 4th ed. Geneva: WHO; 2008.
- Hendricks KA, Wright ME, Shadomy SV, et al. Centers for Disease Control and Prevention expert panel meetings on prevention and treatment of anthrax in adults. Emerg Infect Dis. 2014;20(2):e130687.
- Inglesby TV, O’Toole T, Henderson DA, et al. Anthrax as a biological weapon, 2002: updated recommendations for management. JAMA. 2002;287(17):2236-2252.
- Spencer RC. Bacillus anthracis. J Clin Pathol. 2003;56(3):182-187.
- Mock M, Fouet A. Anthrax. Annu Rev Microbiol. 2001;55:647-671.
- Ministério da Saúde. Guia de Vigilância em Saúde. Brasília: Ministério da Saúde.
- Merck Manual Professional Version. Anthrax.
