Sinal de Koplik
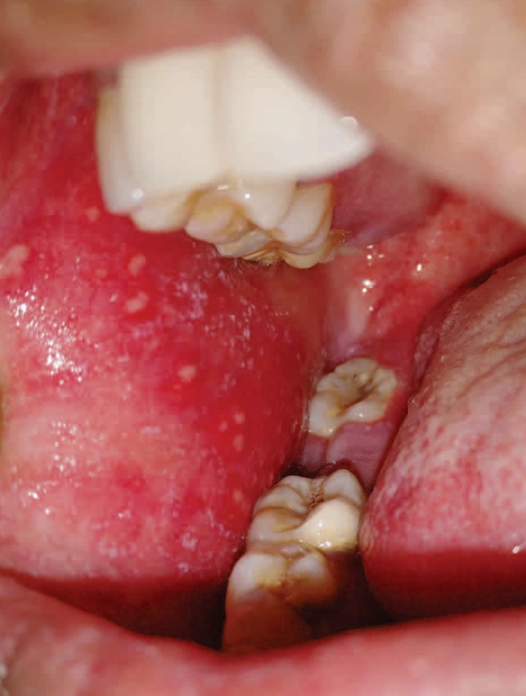
Sinal de Koplik O sinal de Koplik é uma manifestação clássica e precoce do sarampo, caracterizada por pequenas manchas brancas ou cinza-azuladas com base avermelhada, que surgem na mucosa oral, geralmente na altura dos molares. Sua importância clínica está no fato de ser um achado diagnóstico específico do sarampo, aparecendo antes do exantema cutâneo e permitindo o diagnóstico precoce da doença. Fisiopatologia Essas lesões resultam da replicação viral na mucosa oral, seguida por uma reação inflamatória local intensa. O sarampo é causado pelo vírus do sarampo, um membro da família Paramyxoviridae, que atinge as células epiteliais da mucosa respiratória e dissemina-se pelo organismo. A reação inflamatória nas lesões orais reflete a resposta imunológica ao vírus. O sinal de Koplik se apresenta como pequenas lesões puntiformes de 1 a 3 mm, que lembram grãos de areia, frequentemente rodeadas por um halo vermelho. Elas são localizadas na mucosa jugal, próximas aos dentes molares, mas podem se estender para outras áreas da boca. Geralmente, surgem de 1 a 4 dias antes do início do exantema do sarampo e desaparecem rapidamente após o surgimento das manchas cutâneas. Tratamento O tratamento do sinal de Koplik está diretamente relacionado ao manejo do sarampo, uma vez que essas lesões orais representam um dos primeiros sinais patognomônicos da infecção pelo vírus Morbillivirus. Como se trata de uma infecção viral, o tratamento é suporte clínico e sintomático, visando aliviar os sintomas e prevenir complicações. As principais medidas incluem: Hidratação adequada: reposição de líquidos para evitar desidratação. Controle da febre e dor: uso de antitérmicos e analgésicos, como paracetamol ou dipirona, evitando anti-inflamatórios não esteroides (AINEs) devido ao risco de complicações, como a síndrome de Reye. Suporte nutricional: alimentação balanceada e suplementação de vitamina A, especialmente em crianças, pois reduz a morbidade e mortalidade associadas ao sarampo. Isolamento e medidas preventivas: pacientes devem permanecer isolados até pelo menos quatro dias após o surgimento do exantema para evitar a disseminação do vírus. Além disso, é fundamental a imunização como medida preventiva. Pacientes não vacinados devem receber a vacina tríplice viral (sarampo, caxumba e rubéola) ou imunoglobulina em casos específicos, como imunossuprimidos e gestantes expostas ao vírus. O sinal de Koplik desaparece espontaneamente após alguns dias, geralmente antes ou concomitante ao surgimento do exantema cutâneo, sendo um marcador clínico importante para o diagnóstico precoce do sarampo. Quem Descreveu Dr. Henry Koplik Foi descrito pela primeira vez em 1896 pelo pediatra norte-americano Henry Koplik. Ele observou que essas manchas eram um sinal patognomônico do sarampo, ajudando a diferenciar a doença de outras condições febris exantemáticas, como a rubéola. Referências Moss WJ. Measles. The Lancet. 2017;390(10111):2490-2502. doi:10.1016/S0140-6736(17)31463-0. World Health Organization. Measles Fact Sheet. Disponível em: https://www.who.int. Acesso em: dezembro de 2024. Durrheim DN, Crowcroft NS, Strebel PM. Measles – the epidemiology of elimination. Vaccine. 2014;32(51):6880-6883. doi:10.1016/j.vaccine.2014.10.061. Brasil. Ministério da Saúde. Manual de Vigilância Epidemiológica do Sarampo. Disponível em: http://www.saude.gov.br. Acesso em: dezembro de 2024. Deixe um comentário Cancelar resposta Conectado como Dr. Marcelo Negreiros. Edite seu perfil. Sair? Campos obrigatórios são marcados com * Message* Também pode te interessar… SInais Clínicos Sinal de Koplik Dr. Marcelo Negreiros dezembro 30, 2024 SInais Clínicos Sinal de Cullen Dr. Marcelo Negreiros outubro 15, 2024 SInais Clínicos Sinal de Battle Dr. Marcelo Negreiros outubro 13, 2024 SInais Clínicos Sinal do Guaxinim Dr. Marcelo Negreiros outubro 8, 2024